
Titelblatt
Copyright-Seite
Geleitwort
Vorwort
Herausgeber und Autoren
1 Biologie und Physiologie des Implantatlagers unter Berücksichtigung von Transplantationsverfahren
1.1 Einleitung
1.2 Die Zellen des Knochenstoffwechsels
1.2.1 Osteoblasten
1.2.2 Osteoklasten
1.3 Die Kaskade des Knochenumbaus
1.3.1 Zelluläre Kondensation
1.3.2 Zelluläre Differenzierung
1.3.3 Matrixsynthese und -mineralisation
1.4 Biologische Grundlagen der Knochenatrophie und des Volumenverlustes
1.4.1 Genetische Disposition
1.4.2 Lokale schädigende Faktoren
1.5 Biologische Grundlagen der Knochenheilung
1.5.1 Heilung kleiner kortikaler Defekte
1.5.2 Heilung der Extraktionsalveole
1.5.3 Knochenveränderungen während der Heilung
1.6 Der biologische Einfluss der Knochenheilung auf verschiedene Verfahren des Knochenaufbaus
1.6.1 Osteokonduktion, Osteoinduktion und Osteogenese
1.6.2 Die Sinusbodenelevation
1.6.3 Guided bone regeneration
1.6.4 Osteodistraktion
1.6.5 Autogene Knochenblocktransplantation
1.7 Ein Blick in die Zukunft
1.8 Zusammenfassung
1.9 Literatur
2 Der Einfluss der Implantatoberfläche auf die Erfolgsrate von Implantaten in augmentiertem Knochen
2.1 Einleitung
2.2 Klinische Erfahrung
2.3 Diskussion
2.4 Literatur
3 Planung und Diagnostik
3.1 Einleitung
3.2 Patientenberatung
3.3 Anamnese
3.3.1 Nikotinkonsum
3.3.2 Allgemeinmedizinische Befunde
3.4 Spezielle Befunde
3.4.1 Genetische Befunde
3.4.2 Extraoraler Befund
3.4.3 Intraoraler Befund
3.4.4 Radiologischer Befund
3.4.5 Radiologische Verfahren
3.5 Risikoabstufung
3.6 Definition des Behandlungsplans
3.6.1 Wahl der Augmentationstechnik
3.6.2 Augmentationsplanung im zahnlosen Oberkiefer
3.6.3 Augmentationsplanung im zahnlosen Unterkiefer
3.6.4 Augmentationsplanung im teilbezahnten Oberkiefer
3.6.5 Augmentationsplanung im teilbezahnten Unterkiefer
3.7 Implantatplanung
3.7.1 Dreidimensionale Planung
3.8 Diskussion
3.9 Literatur
4 Weichgewebsmanagement während Augmentation, Implantation und Freilegung
4.1 Einleitung
4.2 Instrumentarium
4.3 Weichgewebsmanagement vor Augmentationen
4.4 Weichgewebsmanagement während Augmentation und Implantation
4.4.1 Inzisionen während Augmentation und Implantation
4.4.2 Die Kazanjian-Vestibulumplastik
4.4.3 Die Tunnel-Technik
4.4.4 Freie Bindegewebstransplantate während Augmentation und Implantation
4.4.5 Der palatinal gestielte Bindegewebslappen
4.4.6 Gestielte Periostlappen
4.5 Weichgewebsmanagement bei Freilegungsoperationen
4.6 Weichgewebsmanagement nach prothetischer Versorgung
4.7 Literatur
5 Knochentransplantate aus der Mandibula: Diagnose, Instrumentarium, Entnahmetechniken und chirurgisches Vorgehen
5.1 Einleitung
5.2 Biologische Prinzipien bei der Augmentation mit mandibulärem Knochen
5.3 Techniken zur intraoralen Knochenentnahme
5.3.1 Einleitung
5.3.2 Präoperative klinische und radiologische Diagnostik
5.3.3 Patientenvorbereitung und Entnahmetechniken
5.3.4 Instrumentarium für Knochenentnahmen und Augmentationen
5.3.5 Intraorale Knochenentnahmetechniken zur Rekonstruktion kleiner Defekte
5.3.6 Intraorale Knochenentnahmetechniken zur Rekonstruktion großer Defekte
5.3.7 Ergebnisse
5.3.8 Diskussion
5.4 Augmentationstechniken
5.4.1 Knochendeckelmethode
5.4.2 Erhalt der Extraktionsalveole (Socket preservation)
5.4.3 Augmentation kleiner Knochendefekte
5.4.4 Extensionsplastik, Bone splitting und Bone spreading
5.4.5 Laterale Knochenblocktransplantation
5.4.6 Vertikale Knochenblocktransplantation und 3-D-Rekonstruktionen
5.4.7 Sinusbodenelevation
5.4.8 Lateralisation des N. alveolaris inferior
5.5 Knochenumbildung und Knochenresorption nach der Transplantation
5.6 Schlussfolgerung
5.7 Literatur
6 Extraorale Knochenentnahme
6.1 Einleitung
6.2 Knochenentnahme aus der Calvaria
6.2.1 Patientenvorbereitung
6.2.2 Chirurgisches Vorgehen
6.2.3 Komplikationen
6.3 Knochenentnahme aus der Tibia
6.3.1 Patientenvorbereitung
6.3.2 Chirurgisches Vorgehen
6.3.3 Postoperative Betreuung
6.3.4 Indikation
6.3.5 Komplikationen und postoperative Einschränkungen
6.4 Beckenkammtransplantat
6.4.1 Operationstechnik
6.4.2 Interimsversorgung
6.4.3 Ergebnisse
6.4.4 Komplikationen
6.4.5 Kritische Würdigung
6.5 Literatur
7 Distraktionsosteogenese
7.1 Einleitung
7.2 Geschichte der Kallusdistraktion
7.3 Prinzip der Kallusdistraktion
7.4 Distraktoren
7.4.1 Operationstechnik
7.4.2 Begleitmedikation
7.5 Indikationen
7.5.1 Einzelzahndistraktion
7.5.2 Interforaminale Distraktion
7.5.3 Distraktion im lateralen Unterkiefer
7.5.4 Distraktion bezahnter Segmente (kieferorthopädische Indikation)
7.5.5 Mehrfache Distraktion
7.6 Kontraindikationen
7.7 Ergebnisse
7.7.1 Implantationen
7.7.2 Weichgewebsreaktionen während der Distraktion
7.7.3 Resorptive Veränderungen
7.8 Komplikationen
7.8.1 Schleimhautdehiszenz
7.8.2 Entzündliche Komplikationen
7.8.3 Technische Komplikationen
7.8.4 Sensibilitätsstörungen
7.8.5 Unterkieferfraktur
7.9 Diskussion
7.9.1 Distraktionsrichtung
7.9.2 Komplikationen
7.9.3 Auswahl des Distraktormodells
7.10 Zusammenfassung
7.11 Literatur
8 Komplexe implantatprothetische Rehabilitationen unter dem Aspekt der provisorischen und definitiven Versorgung
8.1 Einleitung
8.2 Besonderheiten der provisorischen Versorgung
8.3 Planung
8.4 Klassifikation der provisorischen Versorgung
8.5 Konzept der definitiven Prothetik
8.5.1 Oberkiefer
8.5.2 Unterkiefer
8.6 Methode
8.6.1 Initiale Behandlungsphase
8.7 Die langzeitprovisorische Versorgung
8.8 Chirurgische Phasen
8.9 Definitive prothetische Versorgung
8.9.1 Erste Sitzung: Repositionsabformung, orientierende Bissnahme
8.9.2 Zweite Sitzung: verblockte Pick-up-Abformung, verschraubtes Zentrikregistrat, arbiträre Gesichtsbogenübertragung
8.9.3 Dritte Sitzung: Funktionsanprobe, Ästhetikanprobe, Überprüfung der Kieferrelation
8.9.4 Vierte Sitzung:Eingliederung
8.10 Kontrollen
8.11 Fazit
8.12 Literatur
9 Komplikationen und Risiken bei augmentativen Maßnahmen
9.1 Einleitung
9.2 Risikofaktoren
9.3 Allgemeine Risikofaktoren
9.3.1 Rauchen
9.3.2 Diabetes
9.3.3 Kortikosteroidmedikation
9.3.4 Bisphosphonat-Therapie
9.3.5 Knochensystemerkrankungen
9.3.6 Hämorrhagische Diathesen
9.4 Lokale Risikofaktoren
9.4.1 Strahlentherapie
9.4.2 Parodontitis
9.4.3 Knochenqualität und Knochenquantität
9.4.4 Weichgewebequalität
9.4.5 Infektionsprophylaxe
9.5 Komplikationen und Risiken bei intraoralen Knochenentnahmen
9.5.1 Knochenentnahme im Rahmen der Implantatbettpräparation
9.5.2 Knochenentnahme im retromolaren Bereich
9.5.3 Knochenentnahme am Kinn
9.6 Komplikationen im Rahmen der Kieferkammextension
9.7 Komplikationen im Rahmen der Sinusbodenelevation
9.7.1 Starke Blutungen
9.7.2 Perforationen der Sinusschleimhaut
9.8 Septum
9.9 Erschwerte Anhebung der Kieferhöhlenschleimhaut
9.9.1 Abszess nach Sinusbodenelevation
9.9.2 Sinusitis
9.9.3 Unvollständige Knochenregeneration nach Sinusbodenelevation
9.9.4 Implantatbettaufbereitung mit Perforation in den Sinus
9.10 Komplikationen im Rahmen von Knochenblockaugmentationen
9.10.1 Fixierung von Knochentransplantaten
9.11 Postoperative Komplikationen
9.11.1 Schmerzen
9.11.2 Blutungen
9.11.3 Schwellung
9.11.4 Hämatome
9.11.5 Candidiasis
9.12 Exposition von Transplantatteilen
9.12.1 Frühexposition
9.12.2 Spätexposition
9.12.3 Exposition nach Implantatinsertion
9.12.4 Schraubenexposition
9.12.5 Membrankomplikationen
9.12.6 Abszess nach Knochenblockaugmentation
9.12.7 Schraubenentfernung
9.13 Komplikationen im Rahmen der Implantatinsertion nach Knochenaugmentation
9.13.1 Unvollständige Transplantateinheilung
9.13.2 Resorption des Transplantates
9.13.3 Einwachsen von Binde- und Granulationsgewebe
9.13.4 Mobilität des Transplantates
9.14 Komplikationen im Rahmen der Implantatfreilegung
9.14.1 Implantatverlust
9.14.2 Transplantatexposition
9.14.3 Blutungen
9.14.4 Lappennekrosen
9.15 Spätkomplikationen nach der prothetischen Restauration
9.15.1 Irritation von augmentierten Bereichen durch prothetische Suprakonstruktionen
9.15.2 Implantatlockerung bei der implantatprothetischen Versorgung
9.15.3 Überwucherung nach Bindegewebetransplantation
9.16 Zusammenfassung
9.17 Literatur

Bibliografische Informationen der Deutschen Bibliothek
Die Deutsche Bibliothek verzeichnet diese
Publikation in der deutschen Nationalbibliografie;
detaillierte bibliografische Daten sind im Internet über
<http://dnb.ddb.de> abrufbar.
ISBN: 978-3-938947-74-6
QUINTESSENZ VERLAG
Postfach 42 04 52; D-12064 Berlin
Komturstraße 18, D-12099 Berlin
Copyright ©2009 Quintessenz Verlags-GmbH, Berlin
Dieses Werk ist urheberrechtlich geschützt. Jede Verwertung
außerhalb der engen Grenzen des Urheberrechts ist ohne
Zustimmung des Verlages unzulässig und strafbar. Dies gilt
insbesondere für Vervielfältigungen, Übersetzungen, Mikroverfilmungen
und die Einspeicherung und Verarbeitung in
elektronischen Systemen.
Lektorat: Peter Rudolf, Quintessenz Verlags-GmbH, Berlin
Herstellung: Ina Steinbrück, Quintessenz Verlags-GmbH, Berlin
Druck: Mercedes-Duck GmbH, Berlin
Printed in Germany
Die zahnärztliche Implantologie hat sich zu einem überaus zuverlässigen und ergebnissicheren klinischen Routineverfahren für all jene Fälle entwickelt, in denen ein in Höhe und Breite adäquates Knochenangebot gegeben ist. Diese Voraussetzung ist jedoch nicht immer erfüllt. Gleichwohl wünschen heute auch Patienten, deren knöcherne Situation das Einbringen von Implantaten eigentlich nicht gestattet, eine Verbesserung der Funktion und der Ästhetik - ja sie erwarten diese sogar als selbstverständlich.
Dieses herausragende Lehrbuch stellt Behandlungstechniken sowohl für Routinefälle als auch für solche dar, die zu dem Schwierigsten gehören, was uns in der zahnärztlichen Praxis begegnet.
Fouad Khoury ist einer der führenden Oralchirurgen und unter diesen zweifelsohne eines der größten Talente. Er verfügt über eine schier unerschöpfliche Erfahrung zu jedem klinischen Aspekt der Transplantatchirurgie und vereint diese mit unbestechlicher Wissenschaftlichkeit. Er verkörpert die ungemein seltene Mischung eines herausragenden Klinikers und eines begnadeten Lehrers.
Für das vorliegende Buch konnte Fouad Khoury ein wunderbares Team von Wissenschaftlern und Hochschullehrern als Mitautoren gewinnen, die ihre Erfahrung und ihr Wissen in gewinnbringender Weise mitteilen. Klar und präzise beschreiben sie ihre Behandlungstechniken und bieten umfangreiche Literaturhinweise am Ende eines jeden Kapitels. Zusätzlich beleuchten sie die interdisziplinären Aspekte der Behandlung - ein Umstand der besondere Beachtung verdient, da allzu viele Kollegen dazu neigen, die Probleme der Patienten nur aus ihrem spezialisierten Blickwinkel zu betrachten. Wir sollten nicht vergessen, ab und zu einen Schritt zurück zu treten und die Behandlung als einheitliches Ganzes zu begreifen, nicht nur als eine bloße Abfolge von Behandlungsschritten, so wichtig jeder einzelne von diesen auch sein mag.
Fouad Khoury ist einer der innovativsten Chirurgen, den ich kenne. Seit Jahrzehnten gehört er zur Avantgarde bei der Entwicklung neuer und kreativer Ideen für die Versorgung seiner Patienten. Seine Innovationen hat er immer rückhaltlos mit der Allgemeinheit geteilt. Dieses Buch ist ein weiteres Beispiel für sein lebenslanges Engagement als Lehrer.
Man kann Fouad Khoury und seine Mitautoren zu dieser herausragenden Arbeit nur beglückwünschen. Sie stellt die zu Papier gebrachte Summe eines ärztlichen Lebenswerkes dar. Wir dürfen sie betrachten, studieren und — das Wichtigste — bei der Behandlung unserer Patienten daraus schöpfen. Indem sie ihr Wissen darüber, welches Vorgehen Erfolg verspricht und welches nicht, mit uns teilen, haben Fouad Khoury und sein Team einen echten Beitrag zur Weiterentwicklung der Zahnheilkunde geleistet. Für all die aufgewandte Mühe sind wir ihnen zu großem Dank verpflichtet.
Prof. Dennis P Tarnow D.D.S.
Direktor der Abteilung
für Parodontologie und Implantologie
am College of Dentistry der New York University
Implantatprothetische Rehabilitationen sind heute ein fester Bestandteil der modernen Zahnheilkunde. Seit ihrer Einführung auf wissenschaftlicher Basis Anfang der 60er Jahre hat sich die Implantologie ständig weiterentwickelt. In Verbindung mit steigenden Patientenwünschen nach ästhetischen und funktionellen Rehabilitationen in den letzten Jahren haben sich parallel dazu verschiedene Augmentationstechniken etabliert, die eine Implantation auch in anatomisch schwierigen Situationen ermöglichen. Implantatprothetische Rekonstruktionen sind heute in vielen Fällen nur noch dank augmentativer Verfahren möglich.
Während der letzten 25 Jahre sind verschiedene Techniken und Materialien für die Rekonstruktion knöcherner Defekte des Alveolarfortsatzes, darunter autogene, allogene oder alloplastische Knochentransplantationen, empfohlen worden. Trotz der Fortschritte im Bereich der allogenen und alloplastischen Materialien sowie der GBR-Techniken, trotz der intensiven Forschung, der Publikationen und positiven Resultate auf diesen Gebieten bleibt die Reproduzierbarkeit und die Zuverlässigkeit solcher Techniken im Vergleich zum autogenen Knochen, der immer noch als Goldstandard gelten darf, sehr begrenzt. Autogener Knochen bietet sowohl mechanische (kortikale) als auch osteogenetische (spongiöse) Eigenschaften, wie sie bisher kein allogenes, xenogenes oder alloplastisches Material erreichen konnte.
Durch die voranschreitende Erforschung und das erweiterte Verständnis der biologischen Prozesse bei der Knochenheilung, -regeneration und -remodellierung in Verbindung mit Transplantationsverfahren ist es inzwischen möglich, fast jeden Patienten mit einer implantatprothetischen Restauration zu therapieren. Der Alveolarfortsatz kann heute funktionell so wiederhergestellt werden, dass eine sichere und korrekte Implantatinsertion auch in Fällen möglich wird, in denen der Knochen stark atrophiert ist. Langzeitergebnisse solcher im augmentierten Knochen inserierten Implantate sind heute mit denen im nicht augmentierten Knochen annähernd vergleichbar.
Für die Augmentation des Knochenvolumens stehen verschiedene Techniken zur Verfügung. In Abhängigkeit von der vorliegenden Situation und Indikation sowie auf der Grundlage einer adäquaten Diagnostik reichen die verschiedenen Möglichkeiten vom minimalinvasiven Verfahren mit lokal entnommenen Knochentransplantaten in Lokalanästhesie bis zum extrem komplizierten Rekonstruktionsverfahren für die 3-D-Wiederherstellung des Kieferkammes mit intra- oder extraoralen Knochentransplantaten.
In diesem Buch sind verschiedene Methoden der Rekonstruktion des Kieferkammes mit autogenem Knochenmaterial dargestellt. Nach einer Übersicht über die Biologie der Knochenheilung sowie über Diagnostik und Planung werden verschiedene Knochenentnahmestellen für autogenen Knochen, wie die Mandibula, die Tibia, der Beckenkamm und die Calvaria, in ausführlicher und verständlicher Form erklärt. Die verschiedenen Abbildungen dokumentieren im Detail die einzelnen Schritte des chirurgischen Vorgehens. Resultate und Langzeitergebnisse werden ebenfalls vorgestellt und diskutiert. Zusätzlich wird das Weichgewebsmanagement in Verbindung mit Knochentransplantationen oder nach der Knochenaugmentation im Detail gezeigt und erläutert. Als mögliche Methode für die Reduzierung des Transplantatexpositionsrisikos wird die Tunnel-Technik vorgestellt.
Auch das prothetische Konzept für die Versorgung von Patienten mit Komplexrestaurationen in Kombination mit multiplen Knochenaugmentationen wird ausführlich und detailliert erläutert. Ein eigenes Kapitel zu den verschiedenen intra- und postoperativen Komplikationen und deren Therapiebeeinflussbarkeit rundet die Darstellung ab.
Das Buch richtet sich besonders an interessierte Implantolgen, die ihren Horizont im Bereich der Transplantationschirurgie auf wissenschaftlicher Basis erweitern möchten.
Abschließend möchte ich allen meinen früheren und jetzigen Mitarbeitern und Freunden, die als Koautoren mit viel Hingabe an diesem Buch mitgewirkt haben, großes Lob und herzlichen Dank aussprechen. Außerdem möchte ich mich bei meinen früheren Mitarbeitern Alessandro Ponte (Turin) und Luca de Stavola (Padova) sowie bei meinen jetzigen Kollegen Pierre Keller und Friedrich-Wilhelm Pape nicht nur für ihre wertvolle Hilfe und Unterstützung bei der Behandlung komplexer Fällen, sondern auch für die präzise Dokumentation und das hervorragende Bildmaterial bedanken.
Zusätzlich möchte ich meinem früheren Mitarbeiter Carsten Becker sowohl für seine wertvolle Hilfe bei der Digitalisierung von Bildmaterial als auch für die schematischen Zeichnungen herzlich danken.
Dank gebührt auch allen namentlich nicht erwähnten Assistenzzahnärztinnen und Assistenzzahnärzten sowie Helferinnen und Technikern der Privatklinik Schloss Schellenstein, die mich bei der Zusammenstellung des Buches unterstützt haben.
Ebenso danke ich dem gesamten Team des Quintessenz Verlages, insbesondere Frau Ina Steinbrück, Herrn Peter Rudolf und Herrn Johannes W. Wolters, für ihre exzellente und professionelle Betreuung.
Mein größter Dank aber geht an meine Ehefrau und meine Kinder, die mich während der Zeit der Bucherstellung großartig unterstützt und stets Verständnis für meine eingeschränkte Freizeit gezeigt haben.
Olsberg, Weihnachten 2008
Fouad Khoury
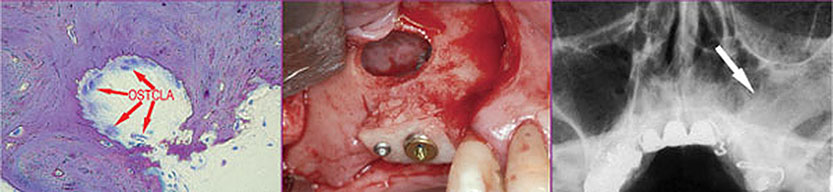
Mit der Einführung enossaler Implantate in die Zahnheilkunde wurde dem Behandler die Möglichkeit eröffnet, auch bei Verlust mehrerer, vor allem strategisch wichtiger Zähne festsitzende prothetische Versorgungen durchzuführen und somit herausnehmbaren Ersatz in vielen Fällen zu vermeiden. Doch waren es zunächst die Menge und die Qualität des Knochens, die die vielfältigen Möglichkeiten implantatgetragener Restaurationen einschränkten. Schon sehr früh nach dem Entfernen von Zähnen zeigt sich zunächst ein Verlust der Breite und anschließend auch der Höhe des Alveolarfortsatzes.20,21 Ein Defizit in der horizontalen Relation konnte durch besondere Implantatformen, wie Blatt- oder Klingenimplantate, ausgeglichen werden, deren Möglichkeiten jedoch beschränkt und deren Langzeitprognosen unsicher waren.59,128 In der Folgezeit wurde ein Vielzahl von Verfahren entwickelt, um verlorenen Alveolarknochen zu regenerieren bzw. zu reparieren.23,88 Hierbei zeigte sich, dass das Verständnis der Anatomie und Physiologie des Knochens von entscheidender Bedeutung für den Einsatz und den Erfolg dieser Verfahren war.157 Ziel dieses Kapitels ist eine Darstellung der Grundzüge des Knochenstoffwechsels zum besseren Verständnis der Transplantationsverfahren.
Eine Beschränkung der Darstellung des Knochenstoffwechsels auf die beiden Zelllinien der Osteoblasten/ Osteozyten und Osteoklasten kann der Komplexität der Vorgänge, an denen eine Vielzahl von Mediatoren, Hormonen, Zellen und Stoffwechselprodukten beteiligt ist, nicht gerecht werden. Dennoch müssen hier zunächst die beiden wichtigsten Zellgruppen des Knochens beschrieben werden.
Osteoblasten gehen aus pluripotenten mesenchymalen Vorläuferzellen hervor (Abb.1-1a). Während der Knochenbildung produzieren sie die Knochenmatrix, aus der durch Mineralisationsvorgänge die Hartsubstanz entsteht. Im Verlauf der Knochenumbauvorgänge werden die Osteoblasten (Abb.1-1b,c) in die Knochenmatrix eingemauert und entwickeln sich zu metabolisch wenig aktiven Osteozyten (Abb.1-1d). Als solche liegen sie jedoch nicht auf Diffusion angewiesen ruhend im Knochen, sondern kontrollieren über Gap junctions der zytoplasmatischen Fortsätze den Ionentransport. Dieser ist ein unentbehrlicher Faktor für die Knochenernährung und diverse Austauschvorgänge, da ein reiner Diffusionsaustausch durch die mineralisierte Matrix eigentlich nicht möglich ist. Die Einschränkung des Ionentransports auf ca. 100µm bewirkt die Beschränkung der Größe von Osteonen auf eben diese Strecke.46 Somit bilden Osteone nicht nur eine strukturelle, sondern auch eine metabolische Einheit (Abb.1-1e, f).
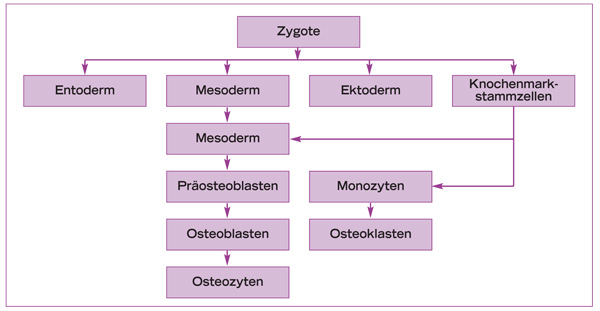
Abb. 1-1a Differenzierung von Osteoblasten und Osteoklasten (nach Nefussi 200799).
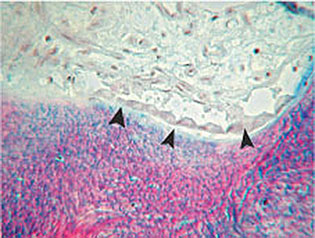
Abb. 1-1b Typische Osteoblasten über einer neu gebildeten Osteoidschicht (Färbung: Masson-Trichrom).
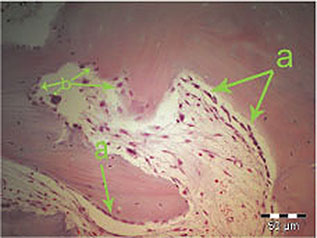
Abb. 1-1c (a) Osteoblastenschichten, (b) Osteoklasten.
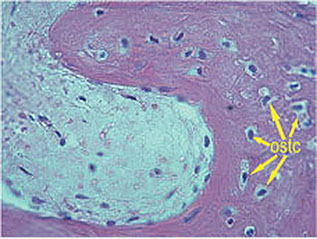
Abb. 1-1d Multiple, vitale Osteozyten (Färbung: Toluidinblau, basisches Fuchsin).
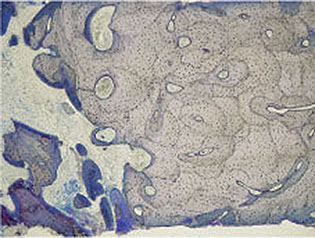
Abb. 1-1e Multiple Osteone: Die Osteozyten sind in einem sehr dichten Havers’schen System eingemauert. Durch die Knochenneubildung verkleinert sich im Laufe der Zeit das Lumen der Havers-Kanäle (Färbung: Thioninblau).
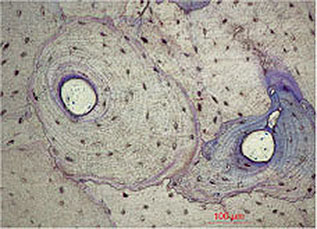
Abb. 1-1f Vergrößerter Ausschnitt aus Abbildung 1-1e.
Auf der Oberfläche des Knochens liegende abgeflachte Osteoblasten werden auch „ruhende Osteoblasten“ oder „Bone lining cells“ genannt (Abb.1-2a). Ihnen werden neben einer Mitwirkung an der metabolischen Aktivität des Knochens auch eine Barrierefunktion und die Kontrolle des Ionenflusses zwischen diesem und dem extraossären Raum zugeschrieben. Zudem spielen sie eine Rolle bei der Regulierung des Knochenabbaus, indem sie Mediatoren freisetzen, die durch Kontraktion der ruhenden Grenzzellen die Oberfläche für die Osteoklasten frei machen und diese selbst zur Resorption aktivieren (Abb.1-2a).58
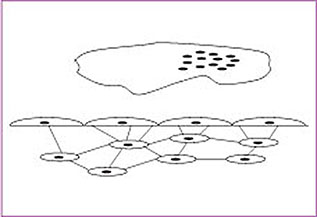
Abb. 1-2a Darstellung einer metabolischen Knocheneinheit: Die Bone lining cells der Knochenoberfläche stehen mit den Osteoblasten in Verbindung. Osteoklasten können an der Knochenoberfläche nicht wirksam werden, solange die Bone lining cells die Oberfläche nicht freimachen (nach Martin 200884).
Im Gegensatz zu den Osteoblasten stammen die Osteoklasten nicht von mesenchymalen, sondern von hämatopoetischen Stammzellen ab.137 Besonders wahrscheinlich scheint eine Herkunft von Granulozyten-Makrophagen-Vorläuferzellen.70,85 Die Osteoklasten bilden eine Gruppe von auf den Abbau kalzifizierter Gewebe spezialisierten Riesenzellen (Abb. 1-2b). Sie finden sich in den sogenannten Howship-Lakunen, Resorptionslakunen im Hartgewebe, und zeigen eine positive Saure-Phosphatase-Reaktion.22,95 Bei einer Zellgröße zwischen 30 und 100µm weisen sie eine Anzahl von ca. 3 bis 30 Kernen auf (Abb. 1-2c). Im acidophilen Zytoplasma zeigen sich Vakuolen, die auf den aktiven Abbauprozess hinweisen.
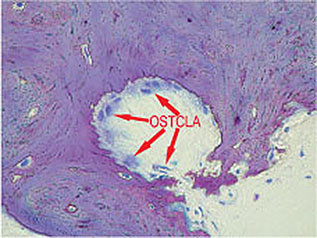
Abb. 1-2b Osteoklasten neben resorbiertem Knochen.
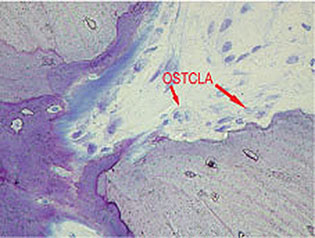
Abb. 1-2c Osteoklasten mit multiplen Nukleonen (Histologie der Abbildungen 1-1e bis 1-1f sowie 1-2b und 1-2c: Dr. D. Moser und Prof. Dr. Dr. R. Ewers, Universität Wien).
Das marginale Areal des Osteoklasten, die klare Zone, befindet sich in Nachbarschaft zum kalzifizierten Gewebe.50 Der zentrale Anteil der Riesenzelle zeigt eine Vergrößerung der Zelloberfläche, das sogenannte „Ruffled border“, das durch Einstülpungen der Zellmembran entsteht. An dieser vergrößerten Oberfläche werden Protonen freigesetzt, die den pH-Wert senken und so die Hartsubstanzen auflösen. Die nach der Auflösung des Hydroxylapatits freiliegenden Kollagenfasern werden anschließend durch lysosomale Enzyme und Kollagenasen abgebaut.147
Für Osteoklasten wurden zwei unterschiedliche Differenzierungswege identifiziert: Der eine ist abhängig von einer Interaktion mit Osteoblasten und erklärt den Wechselprozess von Knochenabbau und -aufbau, der während der physiologischen Knochen-remodellierung stattfindet. Der zweite Weg wird durch Zytokine gesteuert, die während einer Entzündung oder eines Traumas freigesetzt werden, und steht mit dem Knochenverlust bei pathologischen Ereignissen in Zusammenhang. Von den Entzündungsmediatoren sind als besonders relevant für den dentalen Bereich das Interleukin-1 (IL-1) und der Tumor necrosis factor-α (TNF-α) zu nennen.8,56,68 Untersuchungen der letzten Jahre konnten zeigen, dass einige Menschen mit einer verstärkten Freisetzung dieser Mediatoren und somit einem erhöhten Knochenabbau auf entzündliche Reize reagieren.10,69
Die Genetik und Entwicklungsbiologie des Knochenauf- und umbaus wird von Nefussi zu drei wesentlichen Schritten zusammengefasst:61–63,99,153
Am Anfang steht die als zelluläre Kondensation bezeichnete Ansammlung und Reifung zellulärer Massen, die den Ursprung des skelettalen Musters bildet.
Nachdem die Kondensation erfolgreich abgeschlossen wurde, ist der zweite Schritt die Aktivierung und Regulation von Genen, die für die zelluläre Differenzierung verantwortlich sind.
Im letzten Schritt erfolgt die Aktivierung von Genen, die den Prozess der Matrixsynthese und -mineralisierung, die hormonale Aktivität sowie die Adaptation an Strain und Stress durch Remodellierung steuern.
Alle drei Schritte laufen unter Vermittelung durch spezifische Transkriptionsfaktoren ab, die bestimmte Gene aktivieren oder abschalten. Auch nach Abschluss des Knochenwachstums können im Rahmen der Knochenheilung einige dieser Mechanismen aktiviert werden.9,24,39,41,42,152
Der Begriff der zellulären Kondensation bezeichnet eine durch ortsabhängige Transkriptions- und Wachstumsfaktoren induzierte Ansammlung von Zellen zu einer Masse, die die Quelle für die Reparatur des Knochendefekts darstellt. Sie wird durch traumatische Ereignisse jeglicher Form ausgelöst und führt entweder zu einer Entzündung oder zur Degeneration (Abb.1-3). Da die Zellmasse die Quelle für die Reparatur des Knochendefekts darstellt, ist der erfolgreiche Abschluss der Regeneration von der Potenz und Größe der Agglomeration abhängig. Es kann also zu einer Diskrepanz zwischen der Potenz der Zellmasse und dem Ausmaß des zu reparierenden Defektes kommen, die einen Knochenverlust nach sich zieht.
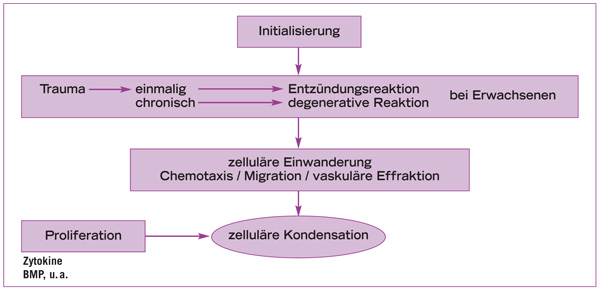
Abb. 1-3 Hauptschritte der zellulären Kondensation (nach Nefussi 200799).
Im zweiten Schritt beeinflussen lokale, ortsspezifische Signalmoleküle der Zellkondensation zelluläre und ZellMatrix-Interaktionen und bewirken die osteogenetische Differenzierung der Zellmassen. Die Zelldifferenzierung bedeutet für die Zelle die endgültige Reifung und führt zu voller Funktionalität. Durch sie entstehen die oben beschriebenen Zelltypen der Osteoblasten/Osteozyten und Osteoklasten.
Die Osteoblasten synthetisieren im wachsenden oder heilenden Knochen Kollagen, Proteoglykane und Glykoproteine, die im Extrazellularraum eine spezifische Quartärstruktur bilden. An dieser Matrix vollzieht sich der Mineralisationsvorgang. Zunächst beginnen die Osteozyten mit der intrazellulären Akkumulation von Kalzium und Phosphat in spezifischen Sekretions-vesikeln, die anschließend aktiv aus der Zelle ausgeschleust werden. Sie enthalten außerdem alkalische Phosphatase. In den Vesikeln bilden sich Apatitkristalle, die sich nach deren Auflösung an den extrazellulären Nukleationsorten (bevorzugt Kollagenfasern und knochenspezifische kalziumbindende Proteine) anlagern.43 In der Mineralisationszone findet sich eine erhöhte Aktivität der alkalischen Phosphatase. Das Fehlen dieses Enzyms ist durch defekte Knochenbildung gekennzeichnet. Nach Abschluss der Mineralisation besteht Knochen zu ca. 65 % aus anorganischer Substanz, hauptsächlich Hydroxylapatit, aber auch Magnesium, Kalium, Chlor, Eisen und Karbonat, sowie zu 25 % aus organischer Substanz und zu 10 % aus Wasser. Die organische Matrix setzt sich aus Kollagen Typ I (90 %) sowie nichtkollagenen Proteinen (z.B. Osteonektin, Osteocalcin, Sialoprotein u.a.) und Lipiden (10 %) zusammen.
Ein insuffizientes Knochenangebot kann prinzipiell zwei Ursachen haben:99 Entweder ist durch eine genetische Disposition das Knochenvolumen am Ort der Implantation vermindert oder lokale schädigende Faktoren haben zu einem Knochenverlust geführt.
Genetische Veränderungen beeinflussen das Knochenwachstum in den verschiedenen Entwicklungsphasen und haben Funktionseinschränkungen ortsspezifischer Signalmoleküle und/oder Transkriptionsfaktoren zur Folge. Meist gehen sie mit Defekten im gesamten dentoalveolären Komplex einher, wobei die Wachstumsdisharmonie einzelner Knochenabschnitte teilweise durch Adaptation kompensiert wird. So führt das präpubertäre Trauma des Unterkieferkondylus mit Einschränkung der Funktion zu einer alveolären Adaptation des homolateralen Alveolarknochens und einem reduzierten alveolären Knochenangebot auf der kontralateralen Seite. Dagegen geht Mikrodontie mit einem unvollständigen Wachstumsreiz des dentoalveolären Komplexes und einem konsekutiven Volumenverlust des alveolären Knochens einher, sodass auch für mögliche Implantationen kein ausreichendes Knochenlager zur Verfügung steht (Abb.1-4a–e).
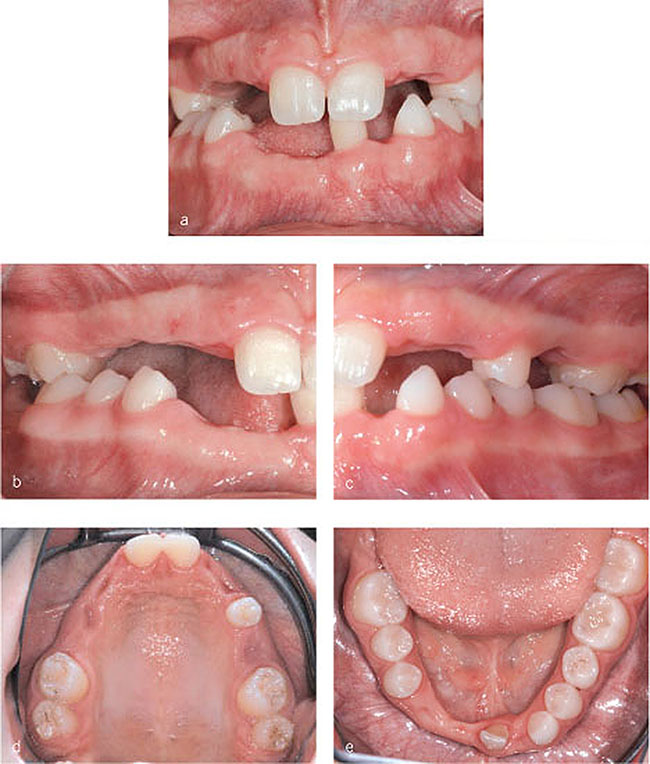
Abb. 1-4a–e Patientin mit Hypodontie. Die Nichtanlage der Zähne 11– 15, 22, 23, 25, 32, 41–43 und 47 hat zu einem deutlichen Volumenverlust des alveolären Knochens geführt.
Störungen in der Phase der Zahnentwicklung führen zu einem lokalen Knochendefizit, was die Theorie unterstützt, dass das regionale Zahnwachstum die Höhe und das Volumen des Alveolarknochens determiniert. Nach dem vollständigen Verlust der Zähne kommt es durch chronisches Fehlen von Strain und Stress zu einem Abbau des Alveolarknochens, bis nur noch der basale Unter- oder Oberkieferknochen zurückbleibt (Abb.1-5a,b).
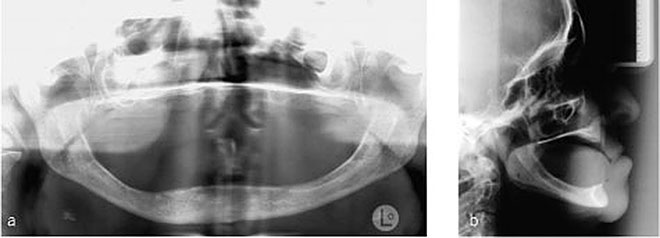
Abb. 1-5a,b Vollständiger Verlust aller Zähne des Ober- und Unterkiefers. Die Patientin trug über mehrere Jahrzehnte einen herausnehmbaren Zahnersatz, was zu einer extremen Atrophie des Ober- und Unterkieferknochens geführt hat.
Der Alveoloarknochenverlust nach Zahnverlust stellt für das Skelettsystem einen singulären Prozess dar. In allen anderen Knochen des Körpers kommt es bei Funktionslosigkeit zu einer Entmineralisierung in Form von Osteoporose, ohne dass dadurch die äußere Form der Knochen in irgendeiner Weise verändert wird. Das heißt, die spongiösen Knochenstrukturen werden reduziert, das kortikale Gerüst bleibt jedoch erhalten. Dagegen führt ein Funktionsverlust des Alveolarknochens zu einer zum Teil vollständigen Involution. Dieser Unterschied ist in der veränderten Funktion nach Zahnverlust zu suchen. Das Kauorgan leitet bei allen Funktionen Strain und Stress in den Alveolarknochen fort, was zu einer periostalen Knochenapposition führt. Umgekehrt kommt es zu einer periostalen Resorption, wenn die Funktion verloren gegangen ist (Abb.1-6a–c).141
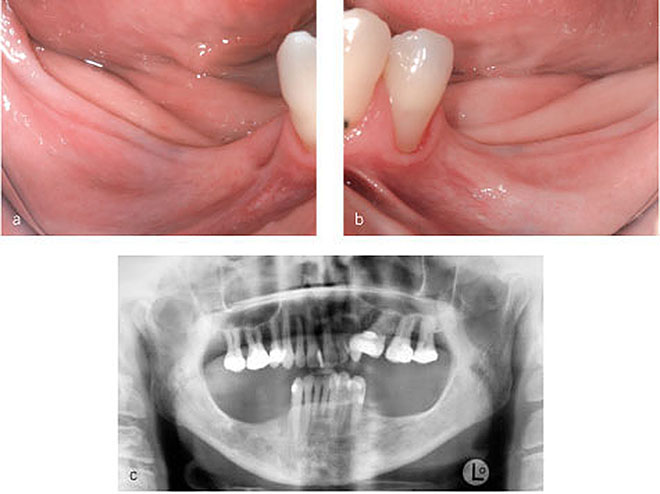
Abb. 1-6a–c Der Verlust der Zähne des Unterkiefer-Seitenzahngebietes hat zu einer deutlichen Breiten- und Höhenreduktion des Alveolarknochens geführt.
Reparative Regeneration findet statt, wenn aufgrund von Unfall oder Krankheit Gewebe verloren geht. Die Stützgewebe des Körpers sind in unterschiedlichem Maß zur Regeneration befähigt. Knorpelgewebe weist so gut wie keine Heilung auf, während Bindegewebe eine gute Heilungstendenz zeigt. Allerdings kommt es hier zu narbiger Heilung und das neu gebildete Bindegewebe hat gegenüber dem Ursprungsgewebe reduzierte Eigenschaften. Einzigartig ist die Reparationsund Regenerationsfähigkeit des Knochens. Innerhalb gewisser Einschränkungen ist eine vollständige Restitutio ad integrum möglich. Hierzu ist jedoch neben mechanischer Stabilität vor allem eine gute Blutversorgung notwendig.
Auch bei der Knochenheilung zeigt der Alveolarknochen im Vergleich mit dem übrigen Skelett einige Besonderheiten. Während dort kleinere Knochenläsionen ohne Verlust repariert werden, kommt es beim Alveolarknochen im Rahmen einer Reparatur immer auch zu einem Volumenverlust. Hierbei muss die Heilung der Extraktionsalveole nach Verlust eines Zahnes von sonstigen traumatischen Ereignissen getrennt und isoliert betrachtet werden.
Die Knochenheilung des Erwachsenen verläuft in ähnlichen Schritten und Kaskaden wie die Knochenbildung (Abb.1-7).41,42,106 Eine partielle Verletzung der versorgenden Gefäße durch das initiale Trauma führt infolge der resultierenden Hypoxämie, unzureichenden Nährstoffzufuhr, Beeinträchtigung des Stoffwechsels und pH-Wert-Absenkung zu zellulärer Nekrose. Aus den Gefäßen werden Blutzellen (Plättchen, Erythrozyten, Leukozyten und Makrophagen) in den Wundbereich freigesetzt. In Verbindung mit den Produkten des Blutplasmas wird auf diesem Wege zunächst ein Blutkoagel gebildet, das für die primäre Hämostase und den Wundschutz sorgt. Die Zellen des Blutkreislaufs werden zur Freisetzung zahlreicher Zytokine angeregt, darunter PDGF, TGF-β, IL-1, IL-6, FGFR-1, FGFR-2, FGF-1, FGF-2, BMP-2 bis -7, TNF-α.72,146,164 Das Zusammenspiel dieser Zytokine und Wachstumsfaktoren, die in bestimmten Konzentrationen und zu bestimmten Zeitpunkten vorhanden sein müssen, bewirkt den Fortgang der Heilung der traumatisierten Bereiche. Hierdurch werden in erster Linie Zellen chemotaktisch angelockt, insbesondere Zellen des Blutkreislaufs und Stammzellen der Stützgewebe, und bestimmte Stoffwechselleistungen aktiviert. Es kommt zur Ausbildung von Granulationsgewebe, zur Neubildung von Gefäßen, schließlich zur Auflösung des Koagels und zum Ersatz durch die Stützgewebe des Körpers.
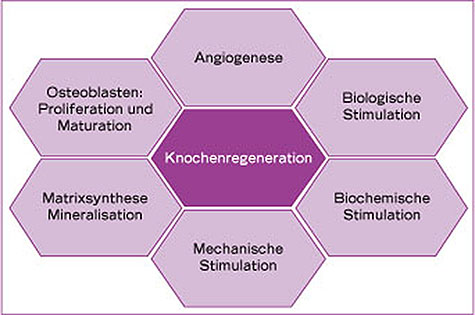
Abb. 1-7 Knochenregeneration: eine komplexe Kaskade mit unterschiedlichen Schwerpunkten (Skript des Maserstudienganges Oralmedizin und Implantologie der Universität Münster).
Die funktionelle Adaptation des Knochens ist ein komplexer, multifaktorieller Prozess, der die kortikale und trabekuläre Architektur bestimmt. Diese wird stets an die lokalen Werte von Stress und Strain angepasst. Jede Veränderung dieser beiden Faktoren führt zu Reaktionen der Zellen des Periostes und Endostes und somit zu Knochenumbauvorgängen. Die primäre Heilung nach einem Trauma erfolgt zunächst ungeordnet und ohne Anpassung der trabekulären und kortikalen Strukturen an die funktionelle Belastung des Knochens. Durch funktionelle Vorgänge wie Kauen und Beißen, die über die Zähne als Strain und Stress auf den dentoalveolären Knochen übertragen werden, kommt es sekundär zur Umstrukturierung des Knochens. Bestimmend für die resultierende Knochenarchitektur (Dicke der Kortikalis, Orientierung, Anzahl und Dicke der Trabekel, Orientierung der Osteone) sind die Intensität und die Frequenz von Strain und Stress.33,34,76,142
Die kortikale Knochenheilung zeigt eine deutliche Abhängigkeit von der Größe des Defekts.57 Defekte, die die Größe eines Osteons (0,2mm) nicht überschreiten, heilen durch direkte Knochenheilung und werden konzentrisch mit lamellärem Knochen gefüllt. In Defekten, deren Größe hierüber hinausgeht, wird zunächst eine Leitschiene aus Geflechtknochen gebildet. In den intertrabekulären Räumen lagert sich lamellärer Knochen ein. Geflechtknochen kann im Gegensatz zu lamellärem Knochen in kurzer Zeit große Defekte überbrücken. Allerdings erfolgt diese schnelle Bildung des Geflechtknochens nur in Defekten einer Größe von bis zu 1mm, die auch als sogenannte „Jumping distance“ bezeichnet wird und eine wichtige Rolle bei der Sofortimplantation spielt.14,48 Die komplette Heilung größerer Defekte erfordert mehr Zeit. Überschreitet die Größe des Defekts 3–5mm, dauert es einige Monate bis zur vollständigen Verknöcherung.
Allerdings bedeutet die vollständige Defektfüllung nicht das Ende der Regeneration. Der neu gebildete Knochen erscheint kompakt, hat aber noch nicht die Festigkeit des originären lamellären Knochens. Durch Havers-Remodellierung kommt es in der Folgezeit zu einem weiteren Umbau, bei dem die primären Osteone durch sekundäre ersetzt werden.
Bei der Heilung einer Extraktionsalveole vollziehen sich die Schritte wie folgt:2,20 In den ersten 3 Tagen nach der Extraktion wird die Alveole weitestgehend durch das Blutkoagel ausgefüllt, dessen Ränder von Entzündungszellen, vor allem neutrophilen Granulozyten, gesäumt sind. Nach 3 Tagen beginnt die Organisation des Koagels, wobei es vor allem von basal durch hochvaskularisiertes Granulationsgewebe ersetzt wird. Im zentralen Anteil des Koagels kommt es zur Lyse der Erythrozyten. Nach 7 Tagen sind die verbliebenen Fasern des Zahnhalteapparates weitgehend aufgelöst. Der Inhalt der Alveole wird bestimmt durch neu gebildete Gefäße, verschiedene weiße Blutkörperchen, mesenchymale Zellen und Kollagenfasern. Zentral zeigen sich Nekrosezonen. Im Bereich des Knochenmarks finden sich Osteoklasten, die die Knochenremodellierung vorantreiben. Nach 14 Tagen liegen die ersten Hartgewebe in der Alveole vor. Hierbei handelt es sich um Geflechtknochen, der in Kontakt mit dem Knochenmark des angrenzenden Alveolarknochens steht. Bereits nach 30 Tagen zeigen sich erste Osteone des Lamellenknochens, die mit dem alten Knochen der Alveole in Verbindung stehen. Der Großteil der Alveole besteht noch aus fibrösem Gewebe, das von einer vollständigen Epithelschicht bedeckt ist. Nach 60 bis 90 Tagen findet man eine Hartgewebsbrücke aus Geflechtknochen, unter der sich bereits neues Knochenmark ausgebildet hat. Sie wird nach 120 bis 180 Tagen durch lamellären Knochen ersetzt. Im Rahmen des Umbaus kommt es bereits in den ersten 8 Wochen zu einem Breiten- und Höhenverlust der Extraktionsalveole (Abb.1-8).2
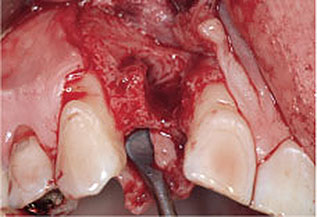
Abb. 1-8 Zustand des Alveolarfortsatzes 8 Wochen nach Zahnextraktion: Die dünne bukkale Alveolenwand ist vollständig resorbiert.
Prinzipiell lassen sich zwei mit Knochenverlust einhergehende Heilungsprozesse unterscheiden: Der eine ist durch ein Defizit an Material für die Neubildung, der andere durch das Fehlen externer Wände gekennzeichnet. Im ersten Fall ist das Volumen, das gefüllt werden soll, durch die umgebenden Wände limitiert und definiert, die Zellen sind aber nicht ausreichend aktiv oder nur in unzureichender Zahl vorhanden. Im zweiten Fall, in dem die äußere kortikale Begrenzung fehlt, muss diese erst definiert werden, was jedoch aufgrund des schnelleren Wachstums der Weichgewebe und der fehlenden Stabilisierung des Koagels nur unzureichend gelingt. Infolgedessen zieht jeder Verlust der externen Kortikalis einen Knochenverlust nach sich, während der Verlust der internen Wände, beispielsweise des Septums, einen solchennicht zur Folge hat. Hieraus wird der entscheidende Einfluss der periostalen Begrenzung auf die Knochenheilung deutlich. Die periostale Oberfläche ist ein ortsspezifisches Signalareal, und die osteoblastären Stammzellen brauchen eine definierte Unterstützung durch Aufrechterhaltung des Raumes, um die originäre Anatomie wiederherstellen zu können. Somit führt der Verlust der externen Kortikalis einschließlich des Periostes zum Verlust entscheidender Signale für die Knochenneubildung. Selbst bei Erhalt des Periostes wird aufgrund fehlender dreidimensionaler Stabilität ein Verlust an Hartsubstanz auftreten.
Wie bereits dargestellt, zeigt Knochen eine hervorragende Regenerationskapazität. Allerdings ist die vollständige Regeneration limitiert, wenn folgende Faktoren die Heilung behindern:
eingeschränkte Blutversorgung
mechanische Instabilität
eine das kritische Maß übersteigende Defektgröße
Kompetition mit hoch proliferativen Geweben.
Um eine befriedigende Knochenheilung im dentoalveolären Bereich zu erzielen, sind verschiedene Verfahren entwickelt worden, mit denen sich die Regeneration des verlorenen Alveolarknochens unterstützen lässt. Alle Verfahren beruhen auf den drei grundlegenden Möglichkeiten der Knochenwiederherstellung: Osteokonduktion, Osteoinduktion und Osteogenese.40,71,144,145
Die Knochenfüllung größerer Defekte wird stark gefördert durch Osteokonduktion, d.h. die Bereitstellung eines Musters oder einer Leitschiene, entlang deren die Knochenzellen den neu gebildeten Knochen ablagern können (Abb.1-9). Hierzu hat das osteokonduktive Material einige Voraussetzungen zu erfüllen: Es muss sich um ein bioinertes oder bioaktives Material handeln. Die Struktur und Porengröße des Materials sollte das Einwachsen des Gewebes und die Knochenapposition fördern.
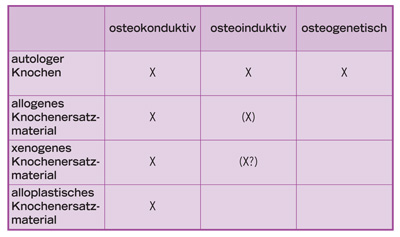
Abb. 1-9 Einteilung der Transplantatmaterialien nach ihren Eigenschaften.
Schließlich sollte das Material idealerweise resorbiert und durch den neu gebildeten Knochen ersetzt werden können. Von den natürlichen Materialen erfüllt spongiöser Knochen am besten die Anforderung an Struktur und Porengröße. Er stellt ein bioaktives und überdies osteogenes Material dar.
Bei der Osteogenese werden mit dem verpflanzten Material natürliche Knochenzellen transplantiert, die von sich aus neuen Knochen bilden können. Voraussetzung hierzu ist eine schonende Handhabung des Transplantats, die verhindert, dass die vitalen Zellen im Verarbeitungsprozess geschädigt werden. Für die Osteogenese kommen deshalb nur autogene Knochentransplantate infrage, da bei Ersatzmaterialien keine Knochenzellen verpflanzt werden und allogene Soforttransplantate sich aus immunologischen und Infektionsrisikogründen verbieten.
16649